תרמודינמיקה תל חי
- 96 שאלות
- 2 תגובות
- 0% הושלמו
- equalizer סטטיסטיקות
- share שתף
מנהלים:

Discuss, Learn and be Happy דיון בשאלות
help
brightness_4
brightness_7
format_textdirection_r_to_l
format_textdirection_l_to_r
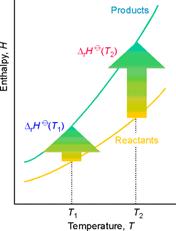
סמן משפטים נכונים בהתייחס לגרף המצורף
1
| done | ||
| done | ||
| done | ||
| done |
a. קיבול החום של התוצרים בוודאות גדול מזה של המגיבים חשבו על זה, אם זה לא היה נכון- הפרש קיבולי החם היה שלילי. אך רק אם הפרש קיבולי החום חיובי, מרווח האנטלפיות בין התוצרים למגיבים יגדל בכיוון החיובי כשהטמפרטורה עולה
b. מתחייב שהפרש קיבולי בין התוצרים למגיבים החום יהיה חיובי נכון: חשבו על זה, רק אם הפרש קיבולי החום חיובי, המרווח בין התוצרים למגיבים יגדל בכיוון החיובי כשהטמפרטורה עולה
g. התהליך הופך ליותר אנדוטרמי כשהטמפרטורה עולה המרווח בין הקווים גדל: יותר הפרש באנטלפיה בכוון החיובי, המשמעות - יותר אנדוטרמי.
h. התהליך אנדוטרמי
מיין לפי
חוק קירחוף מאפשר להעריך את האנטלפיה של ריאקציה בטמפרטורה שאין עליה נתונים בטבלה.
1
| done | ||
מיין לפי
סמן משפטים נכונים על השימוש בחוק הס לאמדן אנלפיית ריאקציה
1
| done | ||
| done | ||
| done |
a. בעזרת חוק הס והנתונים המתאימים ניתן גם לחשב אנטלפיות של ריאקציות שלא באמת מתרחשות נכון. חוק הס הוא כלי חישובי שמאפשר לנו לאמוד "כמה" מבלי לענות על השאלה "האם". לצורך תשובה על השאלה האם ריאקציה מתקיימת באמת או לא, צריך להתייחס לפרמטר אחר שנדבר עליו במהשך הקורס (השינוי באנרגיה החופשית).
d. בחישוב אנטלפיית המראה, ניתן לחבר את אנטלפיית התכה עם אנטלפיית האידוי, כאשר התהליכים מבוצעים באותם תנאי לחץ וטמפרטורה נכון.
e. חוק הס מסתיר בתוכו את העובדה שאנטלפיה היא פונקציית מצב מדוייק. בגלל זה לא חשוב איך אנחנו מגיעים לערך הסופי, ו"מותר" לנו לחלק תהליך לשלבים שנוח לנו לעבוד עימם
מיין לפי
בשיעור דנו ואף ראינו דוגמא על הקשר בין אנטלפיה לאנרגיה פנימית. בעזרת חומר הקורס סמן את המשפט/ים הנכונ/ים
1
| done | ||
| done | ||
| done |
b. כשיש ריאקציה והתהליך מאוד אנדוטרמי או מאוד אקסוטרמי, ההבדל בין שני הפרמטרים זניח
מאוד נכון! אם יש תהליך שמשחרר (לדוגמא) 5000 קילוג'אול למול, אז גם אם חל בו שינוי נפח- בעקבות (לדוגמא) הווצרות מולים נוספים של גז, הרי התרומה שלו (כפי שתבוא לידי ביטוי בהפרש המכפלה לחץ-נפח) תהיה זניחה ביחס לתרומה הבאה מפליטת החום. לכן בקירוב טוב שני הפרמטרים יהיו שווים
e. מכיוון שברוב המקרים התהליכים במעבדה מתרחשים בלחץ קבוע, הרי בריאקציה המתרחשת כולה בנוזלים ההבדל בין הפרמטרים גם אם קיים- זניח נכון. הבדל נפחים בגזים הוא משמעותי. אך במוצקים ונוזלים הוא כמעט תמיד שואף לאפס, ולכן ההבדלים קטנים מאוד עד זניחים
מיין לפי
בסוף המצגת(החוק הראשון של התרמודינמיקה/תרמוכימיה, מתוך מטלה 5) יש מספר שקפים מוסתרים במגוון נושאים הקשורים לתרמוכימיה. עבור על השקפים וסמן את המשפט/ים הנכון/ים (לא מומלץ לנסות לנחש....מדובר על כמה דקות לעבור על השקפים הללו!...)
1
| done | ||
a. גם בתהליך מיהול יש שינוי באנטלפיה עובדתית- כן. נסו למהול חומצה גופריתנית מרוכזת ותראו... ההסבר הוא שתפזורת המים מסביב למולקולות המומס משתנה, וכך למעשה נוצרים ומתפרקים קשרים שדורשים או משחררים חום
מיין לפי
בטבלאות מופיעים חומרים עם קיבול חום שלילי. המשמעות היא שהם תורמים תרומה שלילית לקיבול החום של תערובת חומרים.
1
מיין לפי
במידת הצורך קרא בספר על חוק קירחוף, וענה על השאלה הבאה: הנוסחה המופיע במצגת, מתייחסת להפרש קיבולי החום בחוק קירחוף. עבור נוסחה זו סמן משפט/ים נכון/ים
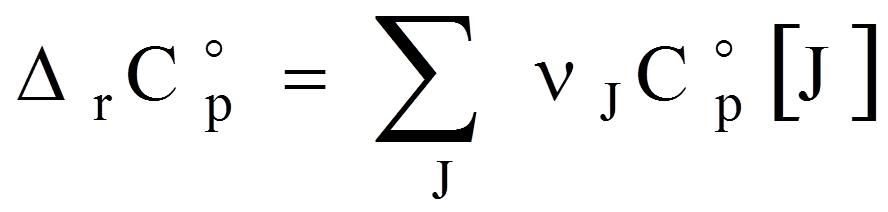
1
| done | ||
| done |
c. המקדם הראשון בתוך סמל ה"סיגמא" מתאר את המקדם הסטויכיומטרי בריאקציה והוא חיובי לתוצרים ושלילי למגיבים המשפט נכון, וכל המוסיף גורע...
d. האינדקס "אפס" מציין תנאי לחץ סטנדרטיים, אך לא בהכרח אומר מה בדיוק הטמפרטורה כן. צריך לזכור שהטמפרטורה הרי לא בהכרח סטנדרטית (אחרת, למה לנו להשתמש בקירחוף?)
מיין לפי
סמן משפט/ים נכונ/ים בנוגע לנושא "תהליכים אדיאבטים הפיכים בגז אידאילי" במצגת "פיתוחים על החוק הראשון"
1
| done | ||
| done | ||
d. בתהליך כזה, אם הנפח גדל הטמפרטורה בהכרח תרד כפי שהוזכר רבות בהרצאה- הטמפרטורה בהכרח תרד. כשהגז מתפשט הוא מבצע עבודה שלילית. מכיוון שאין חום (אדיאבטי) הרי שגם השינוי באנרגיה הפנימית חייב להיות שלילי. זה יקרה רק כשהטמפרטורה תרד!
מיין לפי
השאלה מתייחסת לניסוי ג'אול טומפסון. אנא סמן משפט/ים נכונ/ים
1
| done | ||
| done |
c. השינוי בלחץ בניסוי איננו רציף יש שתי מדרגות לחץ, ואין רציפות (לחץ גבוה מצד אחד ונמוך מצד שני)
d. הניסוי מתבצע תוך העדר שינוי באנטלפיה נכון. ראה הוכחה בחומר
מיין לפי






